
SUIGEN® PCV2 – VẮC XIN PHÒNG BỆNH DO VIRUS CIRCO TYPE 2 ĐẦU TIÊN TRÊN THẾ GIỚI CHỨA KIỂU GEN D
Virus PCV2 thuộc nhóm virus DNA đơn, lây nhiễm ở hầu hết đàn heo trên thế giới và gây thiệt hại kinh tế lớn do tăng tỷ lệ tử vong và chậm tăng trưởng. Chủ động phòng bệnh PCV2 bằng vắc xin là giải pháp chủ yếu để cải thiện năng suất, đặc biệt đối với thể cận lâm sàng, giúp mang lại lợi nhuận một cách rõ ràng (1).
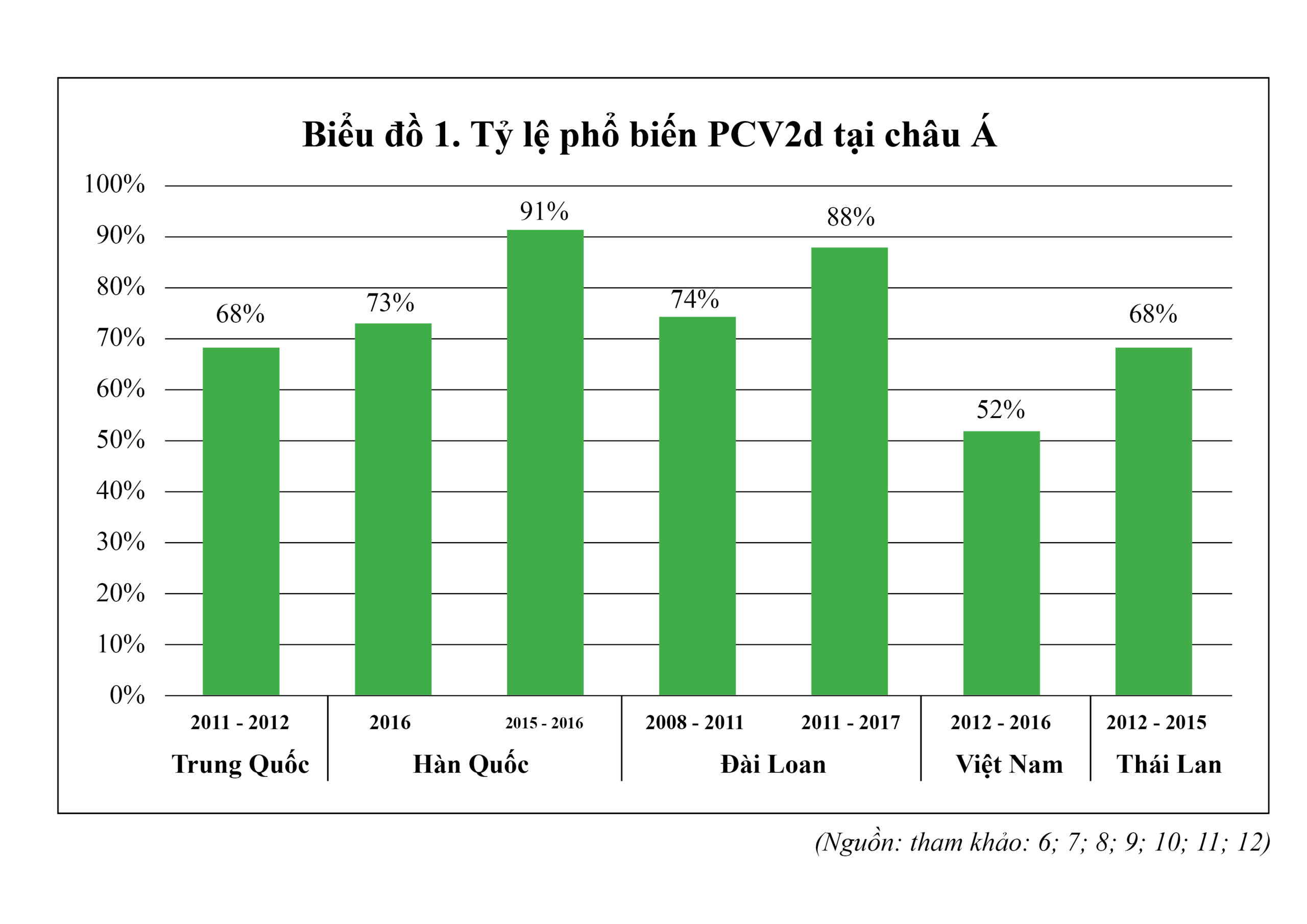
Tỷ lệ đột biến gien của virus PCV2 được ghi nhận là cao nhất trong nhóm virus DNA sợi đơn – gần giống với sự biến đổi của virus RNA sợi đơn – làm cho virus thay đổi nhanh theo thời gian (2-3). Kiểu gien PCV2a chuyển đổi sang kiểu gien PCV2b trong khoảng thời gian 2003 (2). Sự biến đổi này thường có liên quan đến sự gia tăng rõ rệt biểu hiện lâm sàng, tỷ lệ nhiễm và tỷ lệ tử vong tại những nơi mà PCV2b hiện hữu (4). Một nghiên cứu phát sinh loài gần đây, với khoảng 900 giải trình tự gien PCV2 tại 32 quốc gia, đã ghi nhận sự hiện hữu của một đợt biến đổi quan trọng thứ hai, với sự phổ biến và lan truyền của PCV2d thay thế cho PCV2b (5). Tại châu Á, PCV2d đã xuất hiện ở thập kỷ trước và hiện nay trở thành kiểu gien phổ biến ở nhiều quốc gia với tần suất xuất hiện được ghi nhận từ 50% đến 90% (biểu đồ 1).
Sự tiến hóa của PCV2 có mối liên quan lớn đến sự giảm khả năng bảo hộ & loại bỏ mầm bệnh dù đàn heo vẫn được tiêm vắc xin (3). Mặc dù bảo hộ chéo của vắc xin chứa kiểu gien PCV2a được chứng minh, nhưng vẫn xuất hiện những biến đổi thoát khỏi miễn dịch do tiêm vaccine (1).
Ngoài ra, chủng ngừa với vắc xin đồng chủng ghi nhận cho kết quả tốt hơn trong việc giảm tình trạng virus huyết ở một số thử nghiệm về công cường độc (13). Có ít nhất 3 công bố ở Mỹ, Hàn Quốc và Đức ghi nhận các ca lâm sàng của PCV2 trên các đàn heo đang dùng vắc xin để kiểm soát PCV2, liên quan đến việc phân lập được các chủng khác với PCV2b và sau này được xem là PCV2d (14-15-16). Mặc dù thế, kết luận cuối cùng của việc thất bại là do quy trình chủng ngừa, hay do kiểu gien trong vắc xin vẫn còn bỏ ngõ. Do đó, sự phát triển của vắc xin nên dựa theo sự tiến hóa của virus.
Gần đây, một vắc xin (dưới tên gọi Suigen® PCV2) chứa virus kiểu gien PCV2d bất hoạt toàn phần được phát triển, ở dạng pha sẵn với nhũ tương kép (nước/dầu/nước) dùng chủng ngừa cho heo con từ 3 tuần tuổi với 1 liều tiêm bắp duy nhất 1 ml. Vắc xin này đã được kiểm chứng để đánh giá độ an toàn và hiệu quả trong việc tạo lập miễn dịch, kiểm soát tình trạng nhiễm PCV2 và cải thiện năng suất đàn heo.
Bảng 1: Khác biệt về chỉ số miễn dịch, virus huyết và số lượng virus ở hạch bẹn trên 2 mô hình công cường độc khác nhau.
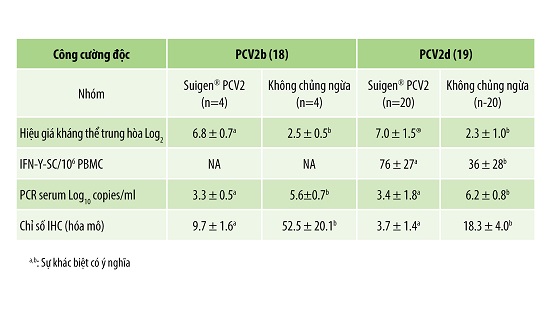
Hai thí nghiệm được thực hiện ở Hàn Quốc cho thấy ở nhóm có tiêm phòng vắc xin Suigen® PCV2 có hiệu giá kháng thể trung hòa và IFN-γ-SC là cao hơn đáng kể, đồng thời tình trạng virus huyết và virus ở mô thấp hơn so với nhóm không được tiêm phòng. Một nghiên cứu thực địa ở Hàn Quốc đã xác nhận rằng nhóm có tiêm chủng vắc xin Suigen® PCV2 có sự giảm đáng kể tình trạng virus huyết và virus ở mô cho đến khi xuất chuồng so với nhóm không được tiêm chủng.
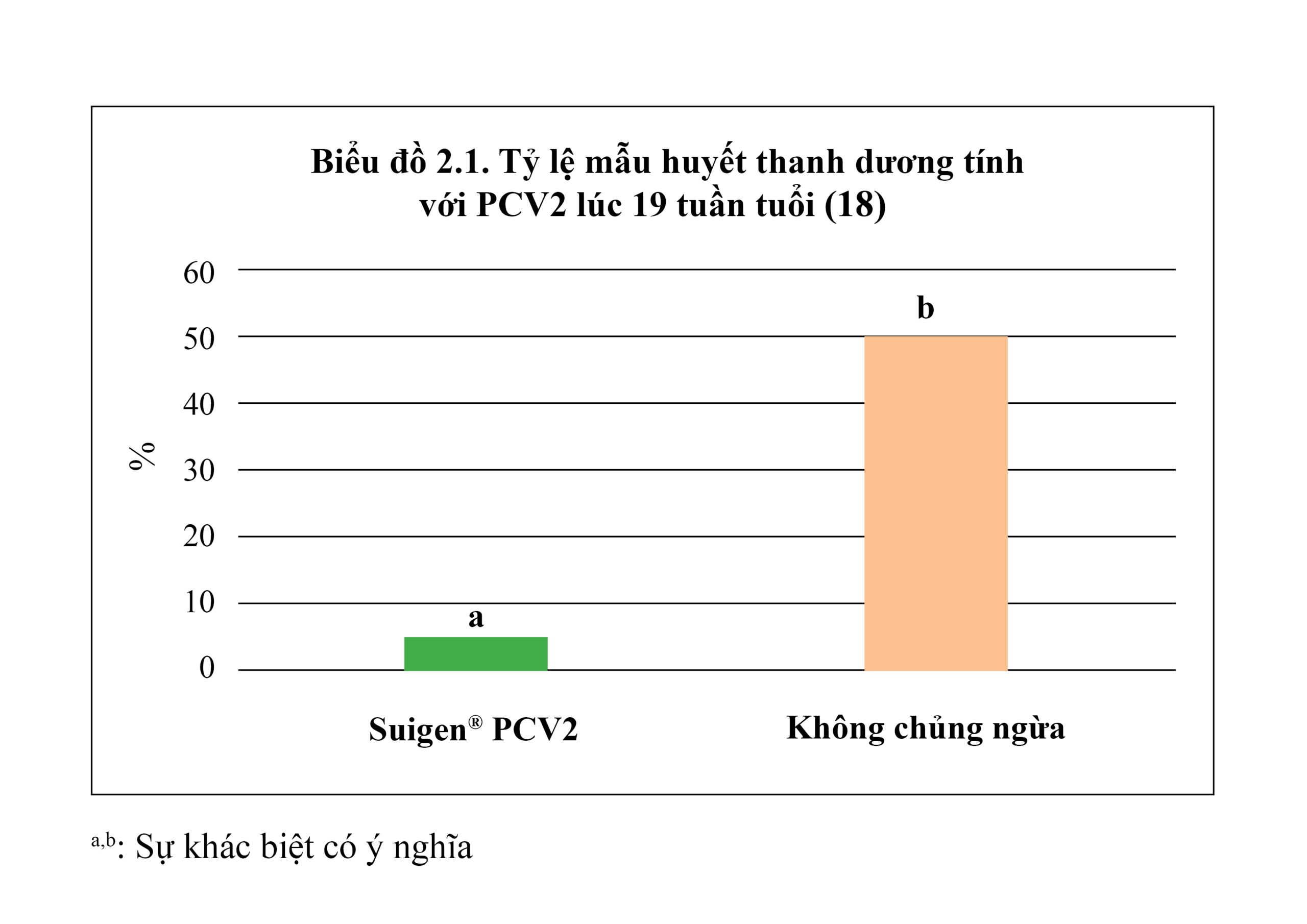
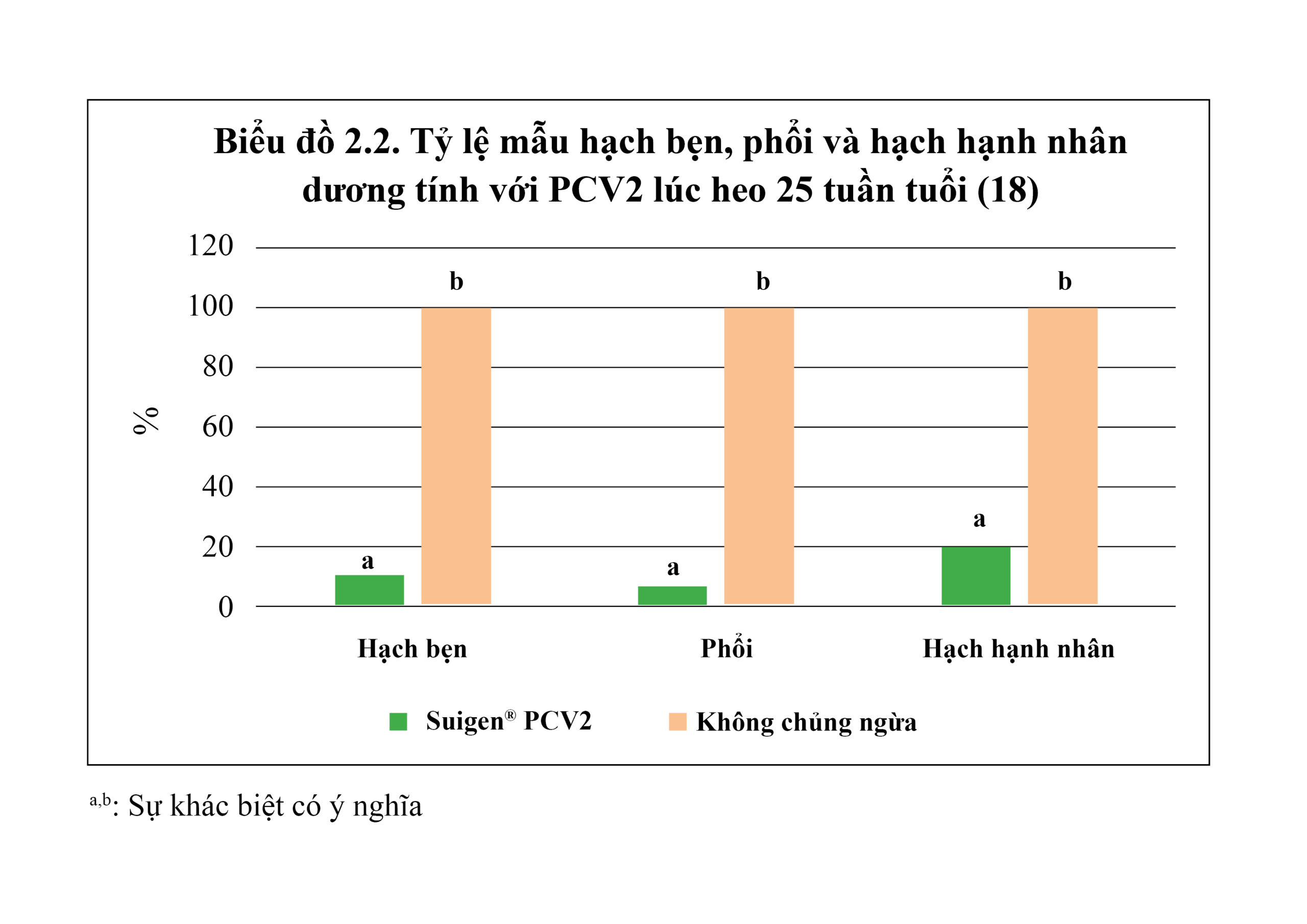
Tỷ lệ dương tính với PCV2 trên mẫu mô của heo được trình bày trong biểu đồ 2.2 cho thấy khả năng bảo vệ rất tốt của vắc xin Suigen® PCV2 khỏi tình trạng nhiễm PCV2 – với sự khác biệt rất có ý nghĩa thống kê – giữa 2 nhóm heo được chủng ngừa và không được chủng ngừa vắc xin Suigen® PCV2. Ngoài ra, kết quả này còn thể hiện hiệu quả miễn dịch kéo dài của vắc xin Suigen® PCV2, có thể bảo vệ heo đến 25 tuần tuổi, nghĩa là đến tận lúc xuất chuồng. Kết quả này trong điều kiện chăn nuôi heo thực tế có ý nghĩa quan trọng hơn là độ dài miễn dịch trong điều kiện thí nghiệm.
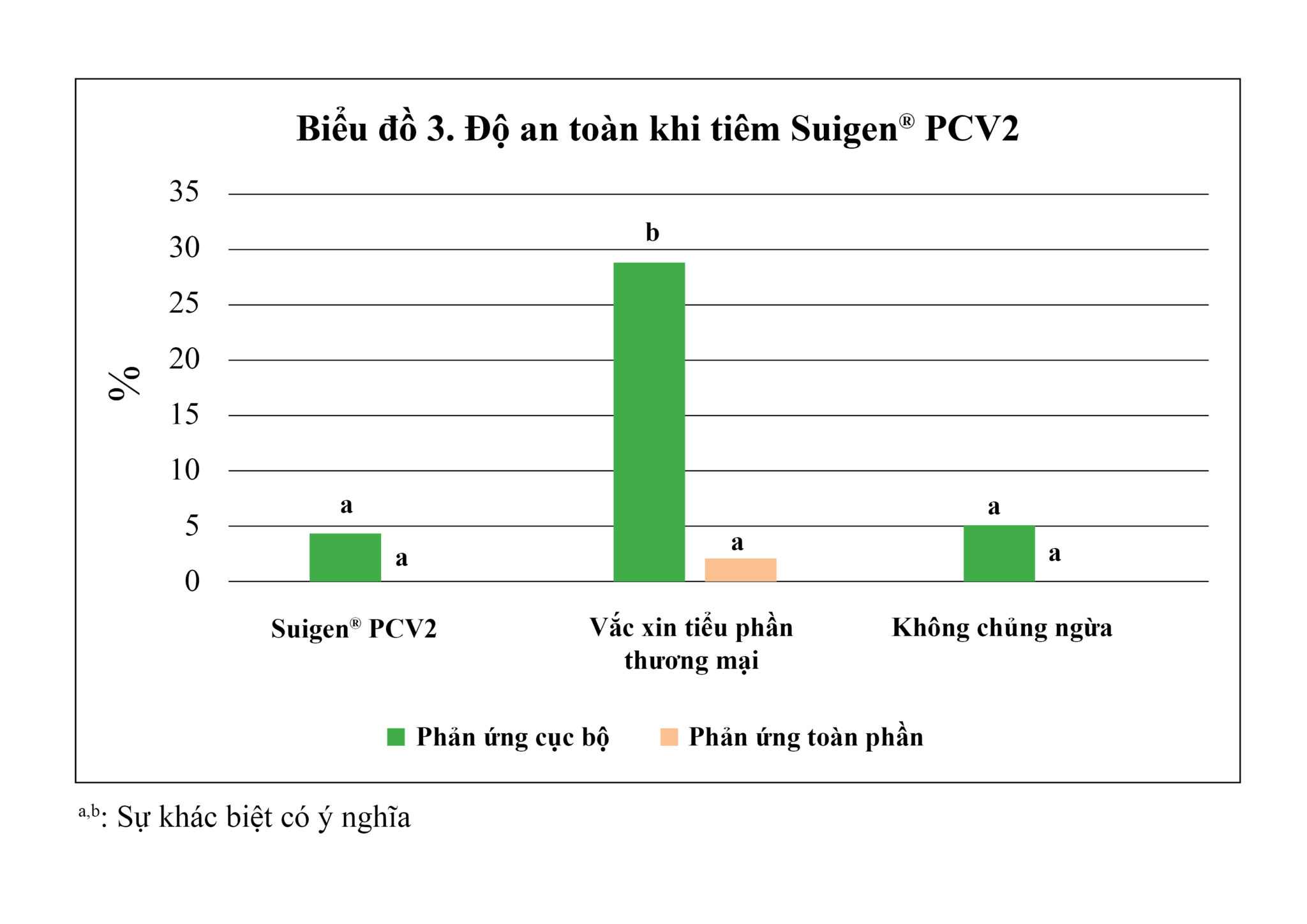
Tính an toàn của Suigen®PCV2 đã được kiểm chứng thông qua 9 thử nghiệm trong điều kiện phòng thí nghiệm và nuôi tại thực địa ở 3 quốc gia (Đài Loan, Hàn Quốc và Philippines: 18-19-20-21) trên 450 heo, bao gồm cả trường hợp tiêm liều gấp đôi (2 ml/ heo). Sau khi chủng ngừa, không có bất kỳ phản ứng toàn thân nào được ghi nhận. Ngoài ra, phản ứng cục bộ cũng không ghi nhận được hay ghi nhận ở mức thấp hơn (tương tự như việc chủng bằng nước muối sinh lý) so với vắc xin tiểu phần (20).
Kết quả của nhiều nghiên cứu tại Hàn Quốc cho thấy sự giảm đáng kể về tỷ lệ tử vong từ cai sữa đến xuất thịt (7.6% so với 12.4%) và cải thiện tăng trọng (78kg so với 73kg lúc heo được 19 tuần tuổi) trên nhóm heo chủng ngừa PCV2 bằng Suigen® PCV2 so với nhóm không được chủng ngừa (18).
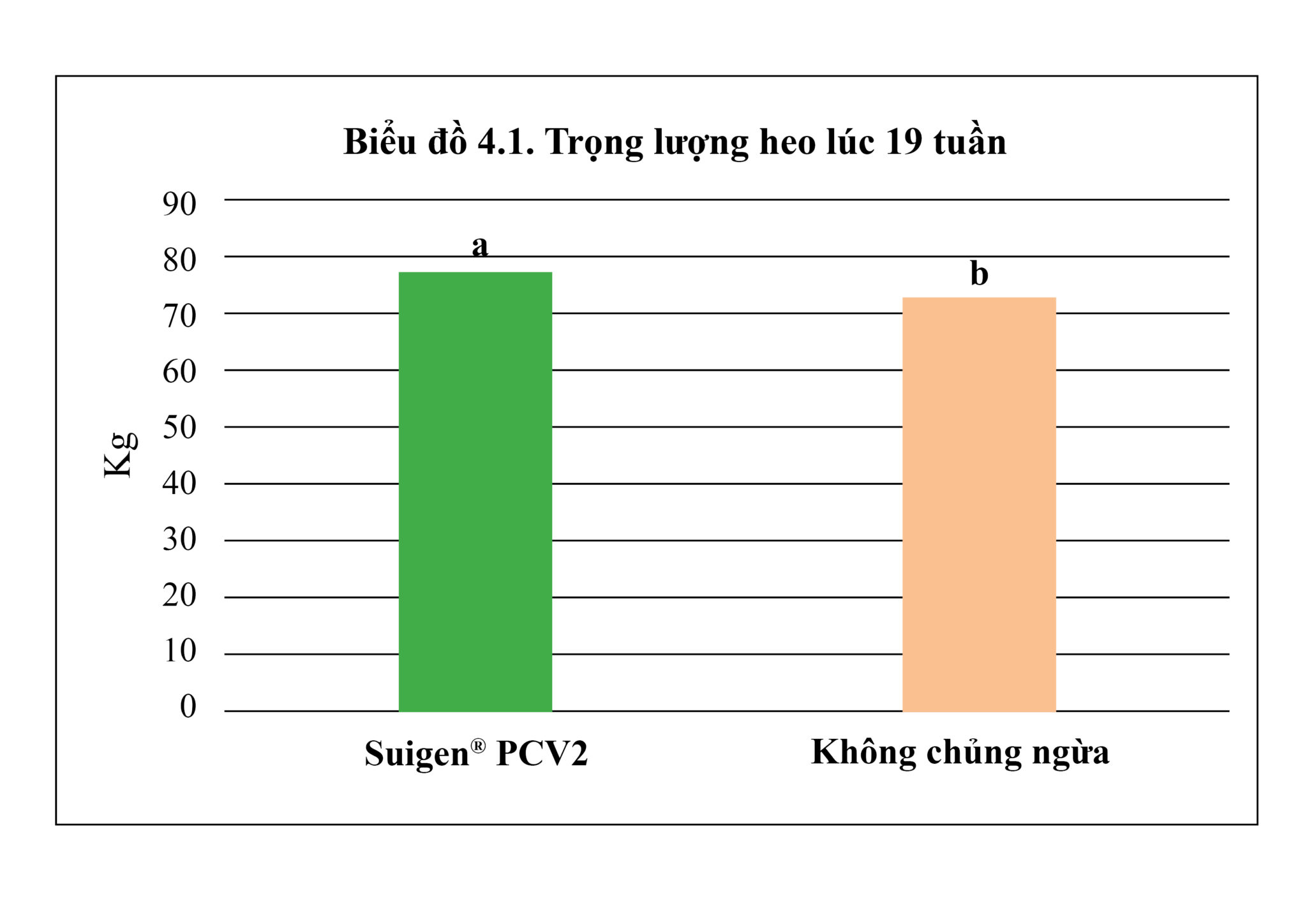
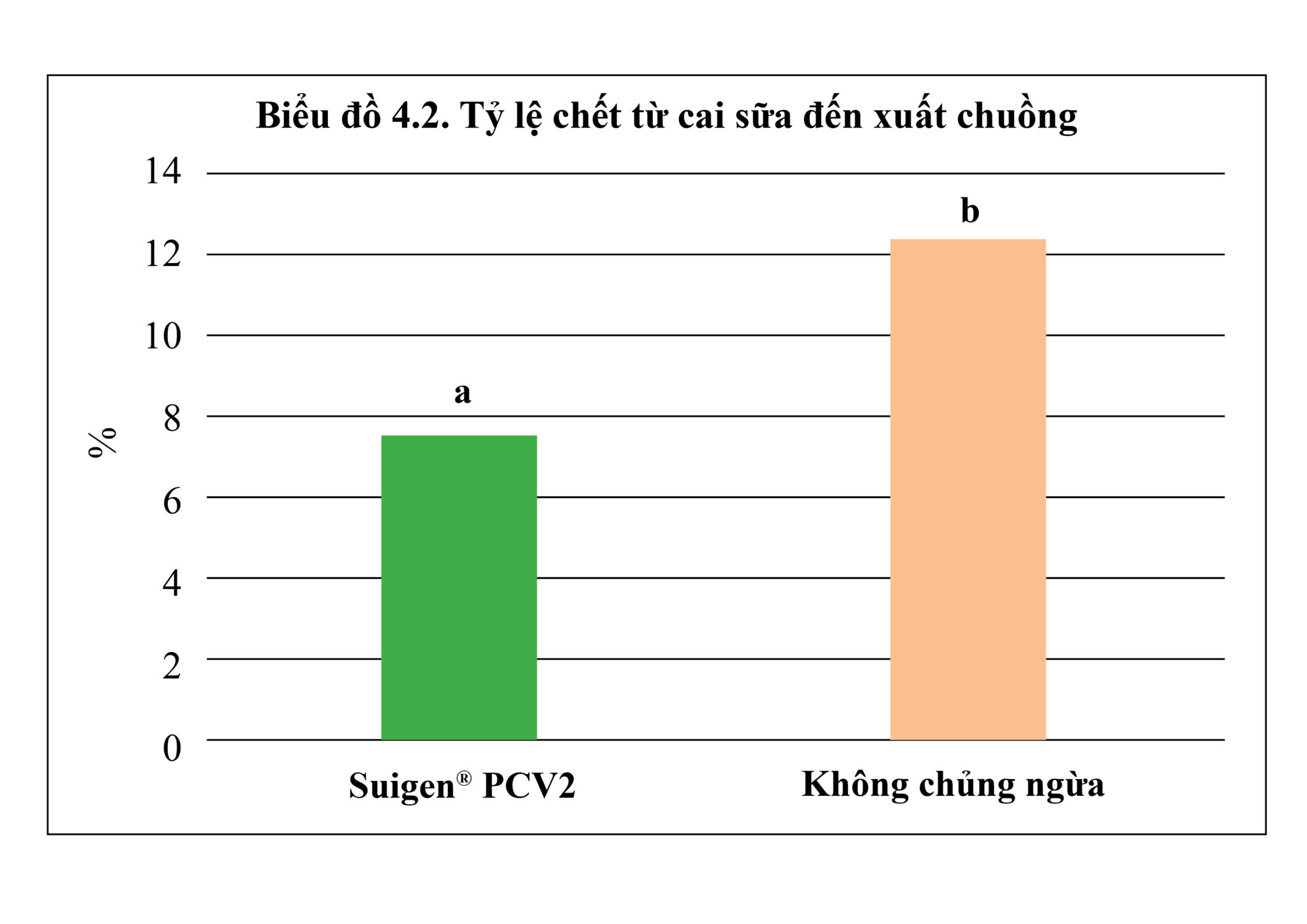
Kết quả của các thử nghiệm đã chứng minh về tính an toàn và hiệu quả của vắc xin Suigen® PCV2 có kháng nguyên là chủng PCV2d (được xem là kiểu gien chiếm ưu thế hiện tại) trong việc kích thích tạo lập miễn dịch đặc hiệu, giảm virus và tăng năng suất đàn heo trên thực tế.
Virbac Việt Nam
Tài liệu tham khảo:
1. Segalés J. Best practice and future challenges for vaccination against porcine circovirus type
2. Experts Rev Vaccines 2015, 14(3): 473-487. 2. Xiao C.T., Halbur P.G. and Opriessnig T. Global molecular genetic analysis of porcine circovirus type 2 (PCV2) sequences confirms the presence of four main PCV2 genotypes and reveals a rapid increase of PCV2d. J. General Virol. 2015, 96:1830-41.
3. Kekarainen T. and Segalés J. Porcine circovirus 2 immunology and viral evolution. Porcine Health Management 2015, 1:17.
4. Xiao C.T., Harmon K.M., Halbur P.G. and Opriessnig T. PCV2d-2 is the predominant type of PCV2 DNA in pig samples collected in the U.S. during 2014-2016. Vet. Microbiol. 2016, 197: 72-77
5. Franzo G., Cortey M., Segalés J., Hughes J. and Drigo M. Phylodynamic analysis of porcine circovirus type 2 reveals global waves of emerging genotypes and the circulation of recombinant forms. Mol Phyl Evol. 2016, 100: 269-280.
6. Wei C., Zhang M., Chen Y., Xie J., Huang Z., Zhu W., Xu T., Cao Z., Zhou P., Su S. and Zhang G. Genetic evolution and phylogenetic analysis of PCV2 infections in southern China from 2011 to 2012. Infection, Genetics and Evolution 2013, 17, 87-92.
7. Kwon T., Lee D.U., Yoo S.J., Je S.H., Shin J.Y. and Lyoo Y.S. Genotypic diversity of PCV2 and genotype shift to PCV2d in Korean pig population. Virus Res. 2017, 228, 24-29.
8. Seung-Chai K., Salik N., Sam K., Jhung-Hyun J., Kyeong-Hwan M., Do-Young J., Chang-Gi J., Amina K., Seog-Jin K. and Won-Il K. The prevalence and genetic characteristics of porcine circovirus type 2 and 3 in Korea. BMC Vet.Res. 2018, 14 :294. Virus research 2009, 145(1):151-156.
9. Chiou M.T., Lin C.N., Yang C.Y., Su G.S., Lin C.F. and Chang T.C. Genotypic change and phylogenetic analysis of PCV2 in Taiwanese pig herds. J. Vet. Med. Sci. 2012, 74, 13031310.
10. Tsai G.T., Yu C.H., Lin C.N. and Chiou M.T. Genetic characterization of porcine circovirus type 2 from Taiwan reveals the emergence of PCV2d-2 since 2008. Proc. APVS 2017, 37.
11. Phuoung L.T.T., Hai N.N., Hong N.T.T., Ngon Q.V., Phuc N.N.H., Hanh T.X. and Dung N.V. Phylogenetic analysis of porcine circovirus type 2 (PCV2) ORF2 from pigs in Vietnam between 2007 and 2016. J. Vet. Sci. Tech. Vietnam Vet. Assoc. 2018.
12. Thangthamniyom N., Sangthong P., Poolperm P., Thanantong N., Boosoongnern A., Hansoongnern P., Semkum P., Petcharat N. and Lekcharoensuk P. Genetic diversity of porcine circovirus type 2 (PCV2) in Thailand during 2009-2015. Vet. Microbiol. 2017, 208, 239-246.
13. Karuppanan A.K. and Opriessnig T. Porcine circovirus type 2 (PCV2) vaccines in the context of current molecular epidemiology. Viruses 2017, 9, 99
14. Opriessnig T., Xiao C.T., Gerber P.F. and Halbur P.G. Emergence of a novel mutant PCV2b variant associated with clinical PCVAD in two vaccinated pig farms in the U.S. concurrently infected with PPV2. Vet. Microbiol. 2013, 163, 177-183.
15. Seo H.W., Park C., Kang I., Choi K., Jeong J., Park S.J. and Chae C. Genetic and antigenic characterization of a newly emerging PCV2b mutant first isolated in cases of vaccine failure in Korea. Arch. Virol. 2014, 159, 3107-3111.
16. Eddicks M., Fux R., Szikora F., Eddicks L., Majzoub-Altweck M., Hermanns W., Sutter G., Palzer A., Banholzer E. and Ritzmann M. Detection of a new cluster of PCV2b strains in domestic pigs in Germany. Vet. Microbiol. 2015, 176, 337-343.
17. Chae C. Commercial porcine circovirus type 2 vaccines: Efficacy and clinical application. Vet. J. 2012, 151-157.
18. Oh Y., Aufa S., Lee W.H., Jeon M.S., Shin C. and Bousquet E. Safety and efficacy trials in piglets of a PCV2 vaccine based on PCV2d genotype. Proc. APVS 2019.
19. Park K.H., Bousquet E. and Chae C. Comparison of a porcine circovirus type 2a (PCV2a)- and PCV2d-based vaccine against a PCV2d challenge. Proc. APVS 2019.
20. Bousquet E., Chen S. P., Lee N., Huang D., Lebreux B. and Fournel S. Comparative safety in piglets of a porcine circovirus type 2 (PCV2) vaccine in field conditions. Proc. APVS 2019.
21. Bousquet E., Aguirre L.M.N., Desamero J., Huang D., Lebreux B., Fournel S., Teran K.C., Robles-Somera I. and Santiago B. Comparative safety and efficacy in sows and piglets of a PCV2 vaccine in Philippine field conditions. Proc. APVS 2019.
