
SỰ BẢO HỘ CHÉO KHÔNG HOÀN TOÀN CỦA VẮC XIN DỰA TRÊN PCV2a ĐỐI VỚI KIỂU GEN PCV2d
Bài viết phân tích hiệu quả bảo hộ chéo của vắc xin PCV2a đối với kiểu gen PCV2d dựa trên các nghiên cứu khoa học quan trọng, bao gồm dữ liệu từ Kang (2020) và Ju (2023), với dẫn chứng cụ thể và giải pháp cải tiến vắc xin trong tương lai.
Porcine circovirus type 2 (PCV2) là một tác nhân gây bệnh nghiêm trọng cho heo, đặc biệt khi kết hợp với các yếu tố stress hoặc bệnh lý khác. Trong số các kiểu gen được xác định, PCV2a và PCV2b từng chiếm ưu thế, nhưng PCV2d hiện đã trở thành kiểu gen phổ biến toàn cầu (Franzo & Segalés, 2020).
1. Tỷ lệ trung hòa kháng thể giữa các kiểu gen
Nghiên cứu của Kang et al. (2020) cho thấy vắc xin PCV2a tạo ra mức kháng thể trung hòa với tỷ lệ 1:4 đối với PCV2d, so với 1:128 đối với PCV2a. Điều này minh chứng rằng hiệu quả bảo hộ chéo giảm đáng kể khi đối mặt với PCV2d.
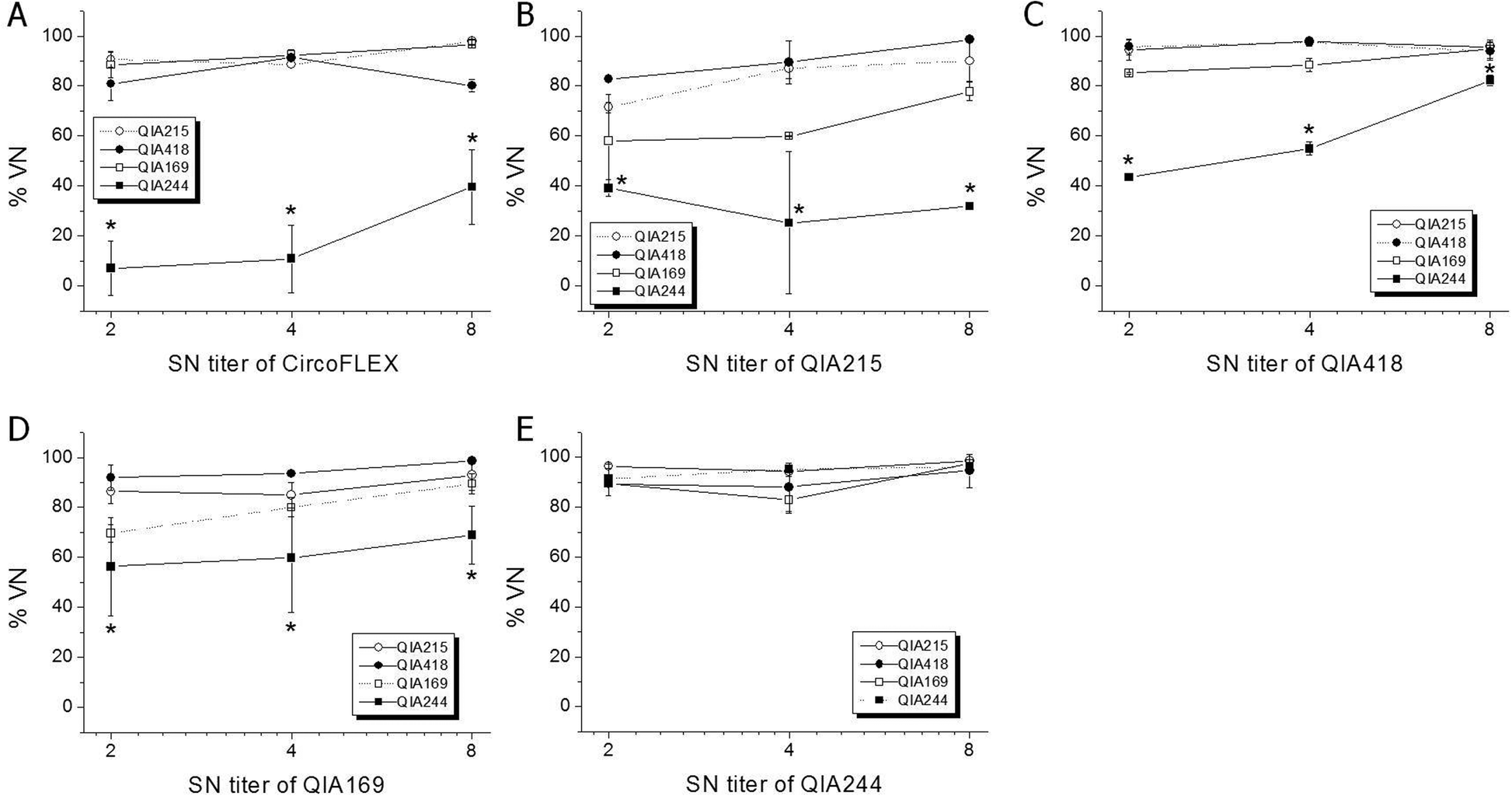
Ghi chú QIA215 (PCV2a), QIA418 (PCV2b), QIA169 (PCV2d), QIA244 (PCV2d), QIA126 (PCV2d)
Hình: Đánh giá khả năng bảo hộ chéo (%VN) giữa các kiểu gen PCV2 khác nhau. Kháng huyết thanh thu được từ chuột lang tiêm vắc xin tiểu đơn vị (a), QIA215 (b), QIA418 (c), QIA169 (d), và QIA244 (e) được trung hòa với bốn chủng virus PCV2: QIA215 (○), QIA418 (□), QIA169 (●), và QIA244 (■). Hiệu quả bảo hộ chéo giữa các kiểu gen được đánh giá bằng kháng huyết thanh có độ pha loãng từ 1:2 đến 1:8 SN chống lại virus đồng chủng (đường chấm). *Khác biệt có ý nghĩa so với đối chứng với p < 0.05.
2. Phân tích miễn dịch học
Ju et al. (2023) nhấn mạnh rằng vắc xin PCV2a chỉ có khả năng bảo hộ không hoàn toàn trước PCV2d. Dù giảm được tỷ lệ nhiễm bệnh, vắc xin này không ngăn chặn hoàn toàn sự lây lan virus trong điều kiện thực địa.
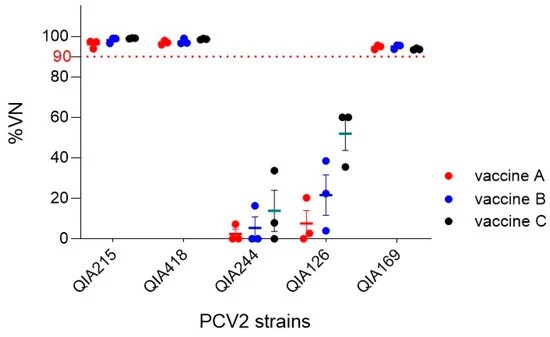
Ghi chú QIA215 (PCV2a), QIA418 (PCV2b), QIA169 (PCV2d), QIA244 (PCV2d), QIA126 (PCV2d)
Hình: Khả năng trung hòa chéo của ba loại vắc-xin dựa trên PCV2a. PCV2a (QIA215), PCV2b (QIA418), PCV2d-1 (QIA244), PCV2d-2 (QIA126), và PCV2d-3 (QIA169) đã được thử nghiệm với các kháng huyết thanh thu thập trên heo (n = 3 cho mỗi loại vắc-xin). Các heo này được tiêm phòng bằng các loại vắc-xin thương mại dựa trên PCV2a (vắc-xin A, B và C). Khả năng trung hòa chéo được biểu thị dưới dạng %VN (trung bình ± SE).
3: Các hạn chế của vắc xin hiện tại
Các nghiên cứu mới nhất đã chỉ ra rằng các vắc xin PCV2a không đảm bảo hiệu quả bảo hộ chéo với PCV2d, chủ yếu do các đột biến kháng nguyên trong protein Cap và sự khác biệt di truyền giữa các kiểu gen (Constans et al., 2015). Điều này cho thấy việc phát triển các vắc xin chuyên biệt cho PCV2d là cấp thiết nhằm kiểm soát tốt hơn sự lây lan trong quần thể heo toàn cầu (Franzo et al., 2024).
1. Đột biến kháng nguyên
PCV2d sở hữu các đột biến tại vùng protein Cap, làm giảm khả năng nhận diện của kháng thể kích hoạt bởi PCV2a (Hou et al., 2019).
2. Tương đồng di truyền thấp
Theo Oh et al. (2019), sự tương đồng di truyền giữa PCV2a và PCV2d đã giảm theo thời gian, làm giảm hiệu quả bảo hộ của vắc xin dựa trên PCV2a.
3. Thay đổi ưu thế kiểu gen
Sự áp lực chọn lọc từ vắc xin PCV2a được cho là đã thúc đẩy sự thay thế PCV2a và PCV2b bởi PCV2d trong đàn heo toàn cầu (Franzo et al., 2020).
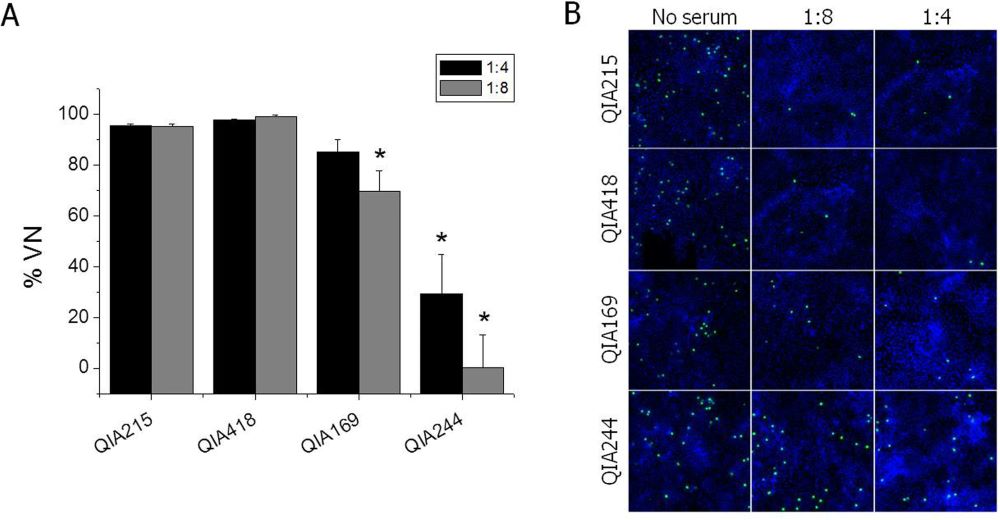
Ghi chú QIA215 (PCV2a), QIA418 (PCV2b), QIA169 (PCV2d), QIA244 (PCV2d)
Hình: Thử nghiệm trung hòa virus sử dụng kháng huyết thanh PCV2 từ heo: a. Kháng huyết thanh (anti-sera) được thu thập từ heo SPF được tiêm vắc-xin PCV2 tiểu đơn vị đã được thử nghiệm trung hòa với các kiểu gen PCV2 đồng chủng và dị chủng. *Khác biệt có ý nghĩa thống kê so với nhóm đối chứng ở mức p < 0,05. b. %VN được chuyển đổi từ số lượng tế bào dương tính với PCV2 được đếm trên mỗi 1 × 10⁴ tế bào sử dụng thiết bị ArrayScan VTI HCS. Nhân tế bào được nhuộm đối quang bằng Heches33258. Các hình ảnh hợp nhất được phóng đại lên 100 lần.
1. Phát triển vắc xin chuyên biệt
Ju et al. (2023) đề xuất rằng việc bổ sung thành phần PCV2d vào vắc xin sẽ nâng cao hiệu quả bảo hộ. Các vắc xin đa giá hiện đang trong giai đoạn thử nghiệm lâm sàng.
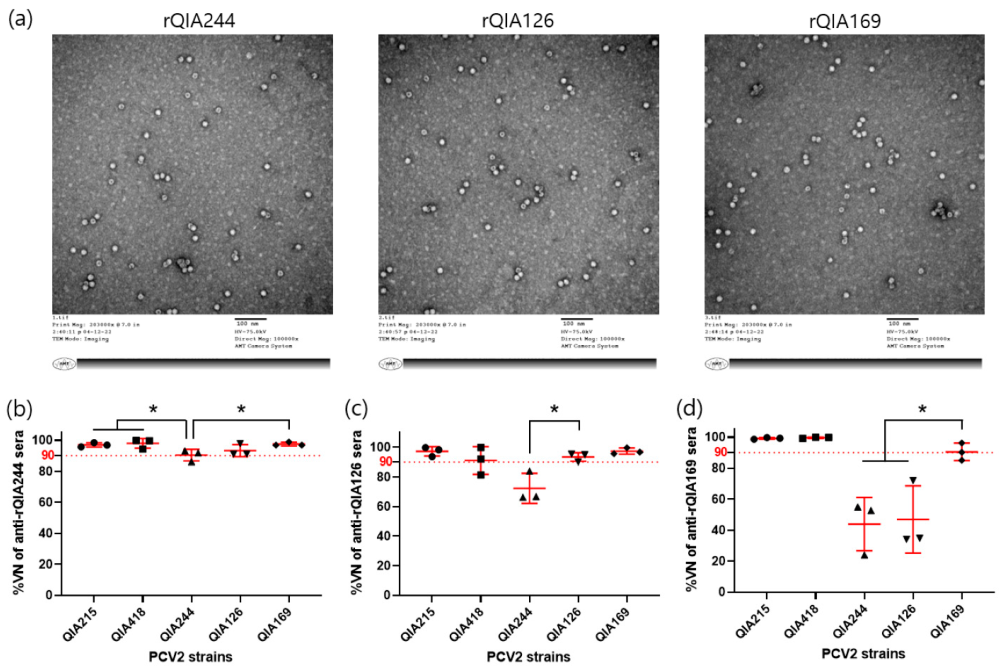
Ghi chú QIA215 (PCV2a), QIA418 (PCV2b), QIA169 (PCV2d), QIA244 (PCV2d), QIA126 (PCV2d)
Hình: Sản xuất VLPs của PCV2d và đánh giá khả năng trung hòa chéo với kháng huyết thanh của các chủng PCV2d trên chuột lang. rQIA244, rQIA126, và rQIA169 được sản xuất bằng hệ thống biểu hiện baculovirus (a). Các chủng PCV2a (QIA215), PCV2b (QIA418), và PCV2d (QIA244, QIA126, QIA169, và QIA416) được trung hòa bằng kháng huyết thanh từ chuột lang được tiêm rQIA244 (b), rQIA126 (c), và rQIA169 (d). Hiệu giá kháng thể trung hoà của kháng huyết thanh chống rQIA244, rQIA126, và rQIA169 được xác định bằng phương pháp VNT90 với chủng tương ứng và áp dụng cho các chủng khác. Khả năng trung hòa chéo được biểu thị dưới dạng %VN (giá trị trung bình ± SE). * biểu thị sự khác biệt có ý nghĩa thống kê (p < 0.05).
2: Ứng dụng công nghệ tiên tiến
Nghiên cứu của Buragohain (2021) và Yoo et al. (2018) nhấn mạnh tiềm năng của công nghệ vắc xin DNA và mRNA trong việc cải thiện hiệu quả miễn dịch. Các vắc xin sử dụng công nghệ này có thể nhanh chóng thích ứng với sự thay đổi của các kiểu gen, đặc biệt là PCV2d.
3. Theo dõi kiểu gen định kỳ
Việc giám sát định kỳ sự tiến hóa của các kiểu gen PCV2 sẽ hỗ trợ điều chỉnh thành phần vắc xin phù hợp với tình hình thực địa (Oh et al., 2022).
Sự bảo hộ chéo không hoàn toàn của vắc xin PCV2a đối với PCV2d đã được chứng minh qua nhiều nghiên cứu. Sự phát triển vắc xin PCV2d không chỉ mang tính khoa học mà còn là một yêu cầu cấp bách nhằm ngăn chặn sự gia tăng các biến thể kháng vắc xin.
Tập đoàn Virbac tự hào giới thiệu Suigen PCV2, vắc xin đầu tiên trên thế giới được sản xuất dựa trên kiểu gen PCV2d. Suigen PCV2 đã được chứng minh cung cấp sự bảo hộ vượt trội và kéo dài hơn so với các vắc xin hiện có, đặc biệt trong bối cảnh kiểu gen PCV2d ngày càng phổ biến và phức tạp trên toàn cầu.
Với kinh nghiệm hơn 50 năm phát triển vắc xin thú y, Virbac không chỉ cam kết mang đến các sản phẩm chất lượng cao mà còn đảm bảo đáp ứng nhu cầu thực tế của ngành chăn nuôi. Suigen PCV2 sẽ là lựa chọn ưu việt và đúng đắn cho các trang trại chăn nuôi, giúp kiểm soát hiệu quả dịch bệnh, giảm thiểu thiệt hại kinh tế và tối ưu hóa năng suất đàn heo.
Tìm hiểu thêm về Suigen PCV2 tại đây: SUIGEN® PCV2 - Giải pháp tối ưu bảo vệ đàn heo trước virus circo loại 2
TÀI LIỆU THAM KHẢO
-
Ju, L., You, S. H., Lee, M. A., Jayaramaiah, U., Jeong, Y. J., et al. (2023). Selection and Evaluation of Porcine Circovirus (PCV) 2d Vaccine Strains to Protect against Currently Prevalent PCV2. Vaccines, 11(9), 1447. https://doi.org/10.3390/vaccines11091447
-
Kang, S. J., Park, K. H., Kim, S., Lee, D., & Chae, C. (2020). Genetic Diversity and Different Cross-Neutralization Capability of Porcine Circovirus Type 2 Isolates Recently Circulating in South Korea. BMC Veterinary Research, 16(1), 1–9. https://link.springer.com/article/10.1186/s12917-020-02549-3
-
Oh, T., Suh, J., Cho, H., Min, K., Choi, B. H., & Chae, C. (2022). Efficacy Test of a Plant-Based Porcine Circovirus Type 2 (PCV2) Virus-Like Particle Vaccine Against Four PCV2 Genotypes (2a, 2b, 2d, and 2e) in Pigs. Veterinary Microbiology, 266, 109348. https://www.sciencedirect.com/science/article/pii/S0378113522001821
-
Hou, Z., Wang, H., Feng, Y., Li, Q., & Li, J. (2019). A Candidate DNA Vaccine Encoding a Fusion Protein of Porcine Complement C3d-P28 and ORF2 of Porcine Circovirus Type 2 Induces Cross-Protective Immunity Against PCV2b and PCV2d Genotypes in Pigs. Virology Journal, 16(1), 1–10. https://link.springer.com/article/10.1186/s12985-019-1156-2
-
Franzo, G., & Segalés, J. (2020). Porcine Circovirus 2 Genotypes, Immunity and Vaccines: Multiple Genotypes but One Single Serotype. Pathogens, 9(12), 1049. https://www.mdpi.com/2076-0817/9/12/1049
-
Opriessnig, T., Karuppannan, A. K., Halbur, P. G., & Calvert, J. G. (2020). Porcine Circovirus Type 2a or 2b Based Experimental Vaccines Provide Protection Against PCV2d/Porcine Parvovirus 2 Co-Challenge. Vaccine, 38(5), 1022–1029. https://www.sciencedirect.com/science/article/pii/S0264410X20300177
-
Karuppannan, A., & Opriessnig, T. (2017). Porcine Circovirus Type 2 (PCV2) Vaccines in the Context of Current Molecular Epidemiology. Viruses, 9(5), 99. https://www.mdpi.com/1999-4915/9/5/99
-
Huan, C., Fan, M., Cheng, Q., Wang, X., & Gao, Q. (2018). Evaluation of the Efficacy and Cross-Protective Immunity of Live-Attenuated Chimeric PCV1-2b Vaccine Against PCV2b and PCV2d Subtype Challenge in Pigs. Frontiers in Microbiology, 9, 455. https://www.frontiersin.org/articles/10.3389/fmicb.2018.00455/full
-
Bandrick, M., Balasch, M., Heinz, A., Taylor, L., & King, V. (2022). A Bivalent Porcine Circovirus Type 2 (PCV2), PCV2a-PCV2b, Vaccine Offers Biologically Superior Protection Compared to Monovalent PCV2 Vaccines. Veterinary Microbiology, 266, 109359. https://link.springer.com/article/10.1186/s13567-022-01029-w
-
Kim, K., Choi, K., Shin, M., & Hahn, T. W. (2024). A Porcine Circovirus Type 2d-Based Virus-Like Particle Vaccine Induces Humoral and Cellular Immune Responses and Effectively Protects Pigs Against PCV2d Challenge. Frontiers in Microbiology, 15, 1334968. https://www.frontiersin.org/articles/10.3389/fmicb.2023.1334968/full
-
Wongchanapai, P., Yamsakul, P., Arunorat, J., et al. (2023). Comparative Efficacy of Chimeric Porcine Circovirus (PCV) Vaccines Against Experimental Heterologous PCV2d Challenges. Veterinary Sciences, 10(2), 80. https://www.mdpi.com/2306-7381/10/2/80
-
Guo, J., Hou, L., Zhou, J., Wang, D., & Cui, Y. (2022). Porcine Circovirus Type 2 Vaccines: Commercial Application and Research Advances. Viruses, 14(9), 2005. https://www.mdpi.com/1999-4915/14/9/2005
-
Segalés, J., & Franzo, G. (2023). Vaccines: Multiple Genotypes But One Serotype. Pathogens, 10(12), 1456. https://www.mdpi.com/2076-0817/10/12/1456
-
Yu, C., Cao, M., Wei, Y., Liu, J., & Zhang, H. (2023). Evaluation of Cross-Immunity Among Major Porcine Circovirus Type 2 Genotypes by Infection with PCV2b and PCV2d Circulating Strains. Veterinary Microbiology, 279, 109521. https://www.sciencedirect.com/science/article/pii/S0378113523001487
-
Buragohain, L. (2021). Development of DNA vaccine against porcine Circovirus type 2 and evaluation ofitsimmuno potential in mice model. Krishikosh eGranth.https://krishikosh.egranth.ac.in/server/api/core/bitstreams/97c569f9-d038-4b72-85d5-8b609298d00f/content
-
Yoo, S.J., Kwon, T., & Lyoo, Y.S. (2018). Challenges of influenza A viruses in humans and animals and current animal vaccines as an effective control measure. Clinical and Experimental Vaccine Research, 7(1), 1–10.https://synapse.koreamed.org/articles/1059500
-
Constans, M., Ssemadaali, M., & Ramamoorthy, S. (2015). Antigenic determinants of possible vaccine escape by porcine circovirus subtype 2b viruses. Biomolecular Insights, 8, 33–42.https://journals.sagepub.com/doi/pdf/10.4137/BBI.S30226
-
Franzo, G., Tucciarone, C.M., & Legnardi, M. (2024). An updated phylogeography and population dynamics of porcine circovirus 2 genotypes: Are they reaching an equilibrium? Frontiers in Microbiology,15,1500498.https://www.frontiersin.org/journals/microbiology/articles/10.3389/fmicb.2024.1500498/full
-
Afolabi, K.O., Iweriebor, B.C., & Okoh, A.I. (2017). Global Status of Porcine Circovirus Type 2 and Its Associated Diseases in Sub‐Saharan Africa. Advances in Virology, 2017, Article ID 6807964.https://onlinelibrary.wiley.com/doi/pdf/10.1155/2017/6807964
- SỰ ƯU VIỆT CỦA VẮC XIN PCV2d SO VỚI VẮC XIN PCV2a HOẶC PCV2b
- SỰ BIẾN ĐỔI CỦA VIRUS PCV2 CÓ PHẢI LÀ NGUYÊN NHÂN DẪN ĐẾN SỰ THẤT BẠI CỦA CHỦNG NGỪA?
- PCV2 THỂ CẬN LÂM SÀNG, ÁC MỘNG CỦA NHÀ CHĂN NUÔI
- MỨC ĐỘ PHỔ BIẾN CỦA KIỂU GEN PCV2d TẠI VIỆT NAM
- LOẠI VẮC XIN PCV2 NÀO PHÙ HỢP CHO TRANG TRẠI CỦA BẠN?
- KIỂM SOÁT BỆNH LÝ HÔ HẤP TRÊN HEO SAU CAI SỮA
- CÓ NÊN TIÊM PHÒNG VẮC XIN PCV2 CHO HEO NÁI
- ĐÁNH GIÁ ĐỘ AN TOÀN VÀ HIỆU QUẢ CỦA VACCINE PHÒNG PCV2 TRÊN NÁI VÀ HEO CON TRONG ĐIỀU KIỆN THỰC ĐỊA PHILIPPINE
- BỆNH HÔ HẤP TRÊN HEO
- BIẾN ĐỔI KIỂU GIEN CỦA PORCINE CIRCOVIRUS TYPE 2 (PCV2) VÀ HIỆU QUẢ VẮC-XIN PHÒNG BỆNH DO PCV2 TRÊN HEO
- SUIGEN® PCV2 – VẮC XIN PHÒNG BỆNH DO VIRUS CIRCO TYPE 2 ĐẦU TIÊN TRÊN THẾ GIỚI CHỨA KIỂU GEN d
- THỬ NGHIỆM ĐÁNH GIÁ VỀ TÍNH AN TOÀN VÀ HIỆU QUẢ CỦA VACCINE PCV2D PHÒNG NGỪA PCV2
- HIỆU QUẢ VƯỢT TRỘI CỦA VẮC XIN SUIGEN DONOBAN-10 PHÒNG 6 VI KHUẨN GÂY HỘI CHỨNG HÔ HẤP PHỨC HỢP TRÊN HEO
- KHẢ NĂNG GÂY BỆNH CAO HƠN CỦA KIỂU GEN PCV2d TRONG BỐI CẢNH TRẠI HEO NHIỄM VIRUS TAI XANH (PRRS)





-resize139x200.png)
